جزوه تایپ شده انتقال جرم و حرارت
دانشگاه پیام نور پارسه علمی کاربردی کارشناسی ارشد دانشگاه آزاد سراسری دکتر ارجمند دکتر غلامسن اسدی دانشگاه صنعتی شریف مهندسی پلیمر
:
:
) (:
//: :
))( *““ ):(
:
( ( ( ) : ))+(( :
((
)))((.
) -( :)( = )(:
:
‘+’- ) ( )( ‘)( =() =() //)(
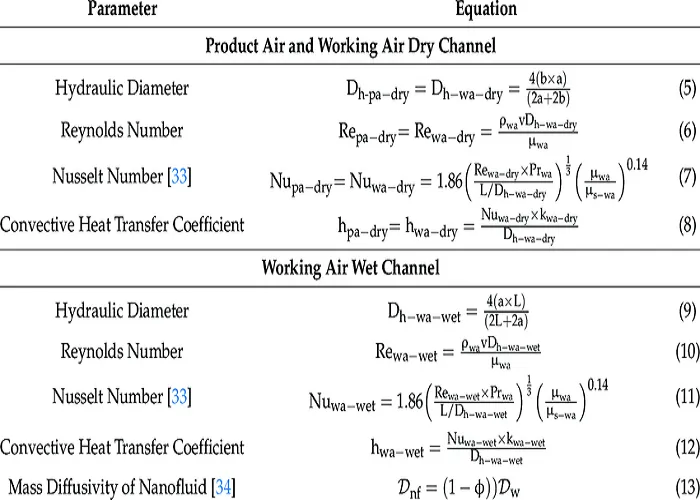
)( ‘:
>)( )( : )(
ِِ() :
= ()
): ( . )( ∑ )( :
ُُ– – – ُُ)()( )(: == =
)()(: ُُ)ُُ( : ) ( دما را در آن نقطه تعیین کنیم.
• اگر گرما از یک سمت وارد شود در نتیجه 0x برابر Q L می شود.
در کُُره یا استوانه بعد مشخصه ، شعاع است.
اگر حرارت در استوانه از سمت قائده)ارتفاع(وارد شود
hیاLجسم را همان Slab در نظر می گیریم. x
عدد بیوت یا بایوت Bi( Biot Number(:
این عدد نشان دهنده نسبت مقاومت جزوه انتقال جرم و حرارت داخلی نسبت به مقاومت حرارتی خارجی است.
???????? ?????? ?????????? مقاومت حرارتی داخلی
=مقاومتحرارتیخارجی
با توجه به رابطه صفحه قبل : در محیط سیال یا واسطه ، مقاومت جابجایی Convection ایجاد می شودو در جسم جامد ، مقاومت هدایتی Conduction ایجاد می شود که عامل محدود کننده در سرعت
در بیوت های بالا یا زیاد ) بیشتر از 47( ، مقاومت خارجی بسیار ناچیز است. در نتیجه سرعت
انتقال حرارت بین سطح جامد و توده سیال بسیار افزایش می یابد ، در چنین زمانی ، دمای سطح جسم به سرعت به دمای توده سیال نزدیک می شود ، بنابراین سیال یا مکانیسم جابجایی ، عامل محدود کننده انتقال حرارت نخواهد بود.
در بیوت های خیلی کم)کمتر از 7.1( مقاومت داخلی یا مقاومت هدایتی بسیار ناچیز است و انتقال حرارت بین سطح و مرکز جسم به سرعت انجام می شود ، به طوریکه در هر زمان ، نقاط مختلف جسم با هم ، هم دما می شوند بنابراین در چنین جسمی ، گرادیان دما نسبت به بُعُد صفر می شود .
برای نشان دادن رابطه دما و زمان در بیوت های کمتر از 6.1 بایستی از رابطه زیر استفاده کرد زیرا طبق گفتههای قبلی ، در بیوت های کمتر از 6.1 ، دما ، در جسم تنها تابعی از زمان است و به موقعیت بستگی ندارد به همین دلیل باید رابطه ای پیدا کنیم که زمان و مکان را نشان دهد:
دما از Ti به T می رسد و جسم در مایعی با دمای Tm جزوه موازنه جرم و انرژی گرفته و دمای جسم در حال زیاد شدن است ، موازنه
q با مکانیسم هدایت وارد جسم می شود در نتیجه رابطه به صورت زیر می شود
انتقال حرارت
رابطه بالا برای پیش بینی پیشینه دمایی ، زمانی که Biot کمتر از 7.1 است می توان استفاده کرد.
اگر فاز جامد را خیلی ریز کنیم )فقط فاز مایع باقی میماند و جامد بسیار ریز می شود ( عدد Biot به کمتر از 6.1 میرسد . به مواد غذایی که خوب همزده می شوند Well mix می گویند.
مثال صفحه 124 PDF :
مثال صفحه 165 :
مسئله برای Biot بالای 96 است چون دمای سطحی از استیک که بر روی سطحی داغ قرار گرفته است ، بلافاصله به دمای سطح داغ می رسد و در این دما باقی می ماند بنابراین می توان در نظر گرفت که مقاومت خارجی وجود ندارد . بنابراین برای حل اینگونه معادلات )بیوت جزوه انتقال جرم و حرارت از 96( بایستی به جدول 16.1 ص162 قسمت معادلات حل شده برای بیوت بالاتر از 96 مراجعه کرد.
1( local الف( a برای استوانه و Slab ب( b برای کُُره 2( mean
در فرمول صفحه قبل Fo دارای متغیر t است.
در رابطه ابتدا n=0 قرار می دهیم و فرمول را محاسبه می کنیم که اگر F0 بیشتر از 6.2 باشد ، همان جمله اول یعنی n=0 دقیق است و نیاز به محاسبه بقیه مقادیر n نیست.
زمانی که گرما از یک سمت وارد می شود 0x از سمتی که گرما وارد نمی شود تاجایی که گرما نفوذ میکند .
مثال 17.5 صفحه 127 :
شیر تغلیظ شده در یک قوطی با قطر 7.5cm و ارتفاع 9.5cm در حال استریل شدن )استریل شدن در بستر( می باشد .زمان مورد نیاز برای اینکه دمای شیر از℃ 95 به ℃115برسد .
a( قوطی به گونه ای دوران دارد که می توان دمای همه نقاط را یکسان فرض کرد .)بیوت کمتر از 6.(
)( : )() ( : ) -( ( ( ( : : )( ، ) ( :
)(.
= = ) (
= - -))( : )(درجه
در این نوع واکنش ها ، سرعت واکنش علاوه بر K به C )غلظت( هم بستگی دارد و سرعت واکنش در همه زمان ها یکسان نبوده و به خاطر رفتار نمایی exp ، در زمان های آغازین، سرعت از بین رفتن یا کاهش بیشتر است و هرچه به انتهای واکنش نزدیک می شویم ، تغییرات غلظت یا سرعت واکنش کمتر می شود زیرا در یک واکنش درجه 1 ، سرعت واکنش به غلظت نیز وابسته است.
نمودار این واکنش به صورت غیر خطی است .
در ابتدا به دلیل غلظت بالا، شیب نمودار زیاد است که با مرور زمان ، غلظت و سرعت و شیب نیز کاهش پیدا می کنند.
در یک واکنش درجه 1 ، رابطه بین غلظت و زمان ، غیر خطی است در حالی که رابطه بین لگاریتم طبیعی غلظت یا lnC و t زمان به صورت خطی می شود ، بنابراین اگر از غلظت های اندازه گیری شده در زمان های مختلف لگاریتم طبیعی) ln( بگیریم و آن را در برابر زمان رسم کنیم خطی نزولی بدست می آید که شیب این خط ، ثابت سرعت واکنش) K( خواهد بود. y a lnCاین کار را برای بدست آوردن K انجام lnC lnbC0 K tx
می دهیم.
تعیین درجه واکنش:
برای این کار ، ابتدا بین غلظت و زمان رگرسیون خطی می گیریم ، اگر R2 )ضریب تعیین( بیشتر از 7.47 باشد )یعنی به احتمال بیشتر از 46 % رابطه بین C و t خطی است( نشان دهنده خطی بودن رابطه می باشد و چنین واکنشی درجه 7 محسوب می شود.
حال اگر 2R کمتر از 6.46 باشد باید در مراحل بعد ، از غلظت های اندازه گیری شده ، لگاریتم طبیعی بگیریم و سپس بین lnC و t رگرسیون خطی بگیریم ، اگر 2R بیشتر از 6.46 باشد ، واکنش درجه 1 است و اگر کمتر از 6.46 باشد سینتیک واکنش ممکن است درجه 2 یا غیره باشد.
در فرآیند های صنایع غذایی اکثر واکنش ها از سینتیک درجه 1 پیروی می کنند و بخشی هم درجه صفر محسوب می شوند مثلا )از بین رفتن M.O ها در اثر حرارت و همچنین تخریب اکثر ترکیبات مغذی درجه 1 محسوب می شوند(.
زمان نیمه عمر) ( half time (t( :
در اکسل برای بدست آوردن معادله خط رگرسیون بایستی روی یک نقطه از نمودار کلیک راست کرده و از منوی باز شده گزینه Add trend line را کلیک می کنیم
برای تعیین D ، ابتدا باید نمونه حاوی M.O مشخصی ، در یک دمای ثابت قرار داده شود و با گذشت زمان تعداد M.O های باقی مانده شمارش گردد سپس در یک نمودار log مقدار باقی مانده در برابر زمان رسم شود ، اگر بین logN و t ، رگرسیون خطی بگیریم و 2R بیشتر از 46 باشد ، از روی شیب خط رگرسیون می توان Dvalue را بدست آورد . .
Dvalue و K به شدت به دما وابسته اند و DT وKT رابطه عکس جزوه انتقال جرم و حرارت. با افزایش دما طبق قانون آرنیوس ، ثابت واکنش از بین رفتن M.O ها ، افزایش می یابد و در نتیجه Dvalue کاهش می یابد .
واحد Dvalue = دقیقه یا ثانیه . واحد K =
اگر منحنی بقا برای یک M.O مشخص در دماهای مختلف رسم شود ، نمودار هایی با شیب های متفاوت بدست می آید که هرچه قدر دما بیشتر شود شیب نمودار بقا نیز بیشتر می شود در نتیجه سرعت از بین رفتن M.O )K(بیشتر می شود در نتیجه Dvalue کاهش می یابد.
– )( % = – = – : ) ∆( ) (. ) (.
)( ، :
:
℃℉)(: -℉؟
:
: ؟
:
) ( ؟
?
فهرست مطالب