جزوه تایپ شده و جامع بیوشیمی عمومی
صنایع غذایی دانشگاه پیام نور علوم آزمایشگاهی دانشگاه آزاد کاردانی تئوری پیام نور محمدی کارشناسی ارشد لنینجر برای آزمون استخدامی هارپر
– – /ً :
() ()
:
(). :
:

ً ؟
٪ (٪)
ً : !
؟
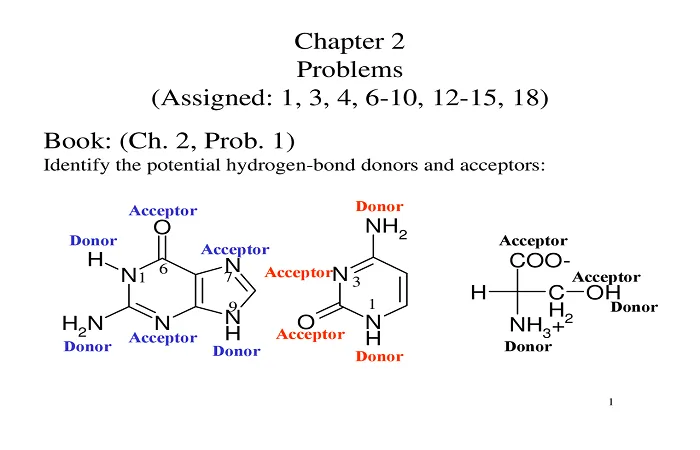
: ٪ – : : : : – – () : () -؛ : : → (++) () (++∆) ++∆: (∆) : (). (++++) () -() () -() () 
() جایگاه فعال انجام می -شود. میدانیم که هر واکنش شیمیایی توسط آنزیم خاصی انجام میشود. به عبارتی دیگر هر آنزیمی سوبستراي خاص خود را شناسایی و آن را به محصول تبدیل میکند. این اختصاصی بودن آنزیم به دلیل ساختار جایگاه فعال است که متناسب با سوبسترا میباشد.
در ارتباط با ساختار جایگاه فعال چند فرضیه مطرح شده است:
مدل قفل و کلید فیشر(Fischer lock and key model) : فیشر درسال 1890 مطرح کرد که جایگاه فعال ساختار سخت و غیر قابل انعطاف دارد که دقیقا مکمل سوبسترا است و سوبسترا در آن قرار میگیرد، مشابه قرار گرفتن قفل در کلید.
ج
هر کدام از این مدلها تا حدودي خصوصیات آنزیمی را توجیه میکند. امروزه ثابت شده است که جایگاه فعال متناسب با حالت گذار سوبسترا (++(S است. در شکل زیر یک واکنش فرضی یعنی نحوه شکسته شدن یک میله توسط آنزیمی که جایگاه فعال آن مشابه حالت گذار است نشان داده شده است.
طبقهبندي آنزیمها
آنزیمها با تمامی تنوعی که دارند در شش گروه طبقهبندي میشوند:
EC = enzyme commission number
1) اکسیدوردوکتازها: واکنشهاي اکسایش و کاهش را کاتالیز میکنند. مهمترین آنها دهیدروژنازها هستند، مانند آنزیم سوکسینات دهیدروژناز:
2) ترانسفرازها: عامل ویژهاي مثل آمین، فسفات و … را از ملکولی به ملکول دیگر انتقال میدهند. مثل آمینوترانسفرازها که گروه آمین را جابهجا میکنند:
3) هیدرولازها: واکنش آبکافت را انجام میدهند، یعنی با اضافه کردن آب پیوند را میشکنند. مثل پپتیدازها که پیوند پپتیدي را میشکنند:
4) لیازها: گروه ویژهاي را بدون واکنش هیدرولیزي از ملکول برمیدارند و یا به ملکول اضافه میکنند. مانند دکربوکسیلازها که گروه کربوکسیل را از ملکلول جدا میکنند:
5) ایزومرازها: واکنشهاي ایزومریزاسیون را انجام میدهند. مثلا تبدیل D -آلانین به L- آلانین توسط آنزیم آلانین راسهماز یا تبدیل گلوکز -6-فسفات و گلوکز-1-فسفات به یکدیگر توسط آنزیم فسفوگلوکوموتاز:
6) لیگازها: بین دو ملکول با مصرف انرژي پیوند کوالانسی ایجاد میکنند. مانند اسیلکوآنزیمA سنتتاز:
سینتیک آنزیمی
آنزیمها به علت ماهیت پروتئینی خود نسبت به دما بسیار حساساند. هر آنزیم در یک دماي خاص داراي بهترین فعالیت است که به آن دماي اپتیمم یا بهینه میگویند. نمودار زیر نشان دهنده تغییر فعالیت آنزیم در برابر تغیرات دما است.
از طرفی هر آنزیم در یک pH خاص داراي بهترین فعالیت است که به آن pH اپتیمم میگویند. نمودار زیر نشان دهنده تغییر فعالیت آنزیم در برابر تغیرات pH است.
طبیعی است که سرعت واکنش آنزیمی با غلظت آنزیم نیز ارتباط مستقیم دارد به نحوي که با افزایش غلظت آنزیم سرعت واکنش آنزیمی افزایش مییابد.
معادله میکائلیس-منتن
در شرایطی که غلظت آنزیم ثابت باشد با افزایش غلظت سوبسترا فعالیت آنزیم افزایش مییابد؛ ولی این افزایش حدي دارد و وقتی غلظت سوبسترا به جایی برسد که تمام ملکولهاي آنزیم از سوبسترا اشباع شوند فعالیت آنزیم دیگر افزایش نمییابد. شکل زیر یک واکنش ساده آنزیمی با کمترین مراحل ممکن را نشان میدهد:
در غلظت ثابت آنزیم(E) با افزایش غلظت سوبسترا (S) میزان کمپلکس آنزیم -سوبسترا (ES) افزایشمییابد تا زمانی که کل آنزیم به صورت ES در بیاید و هیچ آنزیم آزادي (E) وجود نداشته باشد. در اینحالت واکنش آنزیمی با حداکثر سرعت در حال انجام است و با افزایش غلظت سوبسترا سرعت واکنشافزایش نمییابد. به این میزان فعالیت حداکثر سرعت و یا Vmax میگویند. در مورد بسیاري از آنزیمها با رسممنحنی سرعت در مقابل غلظت سوبسترا نموداري به شکل سهمی (هیپربولیک) به وجود میآید که معادله آن به صورت زیر :
=
– () [S] () : (/) () = -= — -:
— – [S] – -: (): () (): ) ((: () () – ()
فهرست مطالب